 |
Синтетическая биология дает возможность создавать биохимические пути для захвата и преобразования углекислого газа или CO2. Исследователи из Института наземной микробиологии Макса Планка разработали синтетический биохимический цикл, который напрямую преобразует CO2 в центральный строительный блок ацетил-CoA. Исследователи смогли реализовать каждый из трех модулей цикла в бактерии E.coli, что представляет собой важный шаг к реализации синтетических путей фиксации CO2 в контексте живых клеток. Разработка новых способов улавливания и преобразования CO2 является ключевым фактором в борьбе с чрезвычайной климатической ситуацией. Синтетическая биология открывает возможности для разработки новых для природы путей фиксации CO2, которые улавливают CO2 более эффективно, чем те, которые были разработаны в природе. Однако реализация этих новых для природы путей в различных системах in vitro и in vivo все еще представляет собой фундаментальную проблему. Теперь исследователи из группы Тобиаса Эрба разработали и сконструировали новый синтетический путь фиксации CO2, так называемый цикл THETA. Он содержит несколько центральных метаболитов в качестве промежуточных продуктов, а его выходом является центральный строительный блок, ацетил-CoA. Эта особенность позволяет разделить его на модули и интегрировать в центральный метаболизм E. coli. Весь цикл THETA включает 17 биокатализаторов и разработан на основе двух самых быстрых из известных на сегодняшний день ферментов, фиксирующих CO2: кротонил-CoA карбоксилазы/редуктазы и фосфоенолпируваткарбоксилазы. Исследователи обнаружили эти мощные биокатализаторы в бактериях. Хотя каждая из карбоксилаз может захватывать CO2 в 10 раз быстрее, чем RubisCO, фермент, фиксирующий CO2 в хлоропластах, эволюция сама по себе не объединила эти способные ферменты в естественном фотосинтезе. Цикл THETA превращает две молекулы CO2 в одну молекулу ацетил-КоА за один цикл. Ацетил-CoA является центральным метаболитом почти во всех видах клеточного обмена и служит строительным блоком для широкого спектра жизненно важных биомолекул, включая биотопливо, биоматериалы и фармацевтические препараты, что делает его соединением, представляющим большой интерес для биотехнологических приложений. Сконструировав цикл в пробирках, исследователи смогли подтвердить его функциональность. Затем началось обучение: благодаря рациональной оптимизации с помощью машинного обучения в ходе нескольких раундов экспериментов команда смогла повысить выход ацетил-CoA в 100 раз. Для того чтобы проверить его применимость в естественных условиях, необходимо поэтапно внедрить его в живую клетку. Для этого исследователи разделили цикл THETA на три модуля, каждый из которых был успешно внедрен в бактерию E. coli. Функциональность этих модулей была проверена с помощью селекции, связанной с ростом, и/или изотопного мечения.
Замыкание цикла THETA все еще представляет собой серьезную проблему, поскольку все 17 реакций должны быть синхронизированы с естественным метаболизмом E. coli, который, естественно, включает в себя от сотен до тысяч реакций. Однако демонстрация всего цикла in vivo — не единственная цель, подчеркивает исследователь.
«Внедрение частей цикла THETA в живые клетки — важное доказательство принципа синтетической биологии», — добавляет Тобиас Эрб. „Модульная реализация этого цикла в E. coli открывает путь к реализации очень сложных, ортогональных, новых для природы путей CO2-фиксации на клеточных фабриках. Мы учимся полностью перепрограммировать клеточный метаболизм, чтобы создать синтетическую автотрофную операционную систему для клетки“. 02.01.2024 |
Биосфера
 | |
| Горные деревья спасаются от потепления, сползая и поднимаясь по склонам | |
Деревья в бразильском Атлантическом лесу ... | |
 | |
| Казанские ученые заявили, что адаптивность молочного скота важнее генетики | |
Исследователи из Казанского государственн... | |
 | |
| Учёные предлагают контролировать москитов с помощью генетической селекции | |
Исследователи из Virginia Tech нашли новы... | |
 | |
| Scientific Reports: Экологичное лечение спасает яйца кальмаров от паразита | |
Выращивать кальмаров в аквакультуре пытаю... | |
 | |
| Animal Behaviour: Собаки лучше свиней реагируют на звуки человека | |
Способность собак чувствовать боль человека мо... | |
 | |
| PRSBBS: Несколько видов муравьев выработали одинаковые отношения с деревьями | |
Муравьи известны своим сложным социальным пове... | |
 | |
| Студенты СевГУ предложили способ найти сбежавшую собаку при помощи спутника | |
Студенты второго курса Института радиоэлектрон... | |
 | |
| Scientific Reports: Кошки до того похожи на людей, что помогут лечить ожирение | |
Домашние кошки могут помочь в изучении ож... | |
 | |
| Палеонтологи: в Калининградской области росли пальмы, секвойи и дубы | |
Калининградская область — регион с&... | |
 | |
| Ученые СПбГУ: Бактериальные споры способны пережить падение из космоса | |
Математики Санкт-Петербургского государственно... | |
 | |
| Учёные БФУ участвовали в изучении миграций морских позвоночных в позднем мелу | |
Учёные Балтийского университета имени Канта вм... | |
 | |
| Animal Biotelemetry: Меховые метки улучшат технологию слежения за медведями | |
Благодаря новым приборам для отслеживания... | |
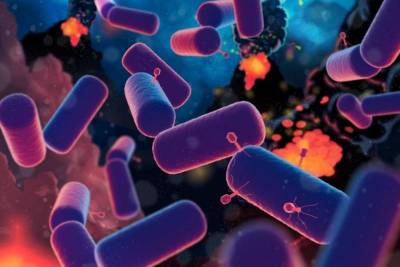 | |
| Nature Ecology & Evolution: Всеобщий предок LUCA оказался старше, чем считалось | |
Международная группа исследователей под р... | |
 | |
| Cell: Впервые восстановлена трёхмерная структура хромосом шерстистого мамонта | |
Учёные из Дании и США впервые в... | |
 | |
| Геоботаники СПбГУ бьют тревогу: азиатские дубы угрожают флоре Абхазии | |
Ученые из Санкт-Петербурга выяснили, что&... | |
 | |
| Frontiers in Veterinary Science: Открыт способ отучить кошек царапать мебель | |
Многие владельцы кошек сталкиваются с тем... | |
 | |
| Ученый объяснил, как планктон выживает в турбулентных потоках | |
Как движутся частицы в турбулентных жидко... | |
 | |
| Останется ли магний снотворным для кузнечиков в результате потепления? | |
Соединения магния — распространенны... | |
 | |
| Увидеть живьем — большая удача: натуралист снял в Казани скрытное насекомое | |
В последние дни апреля во время лесн... | |
 | |
| FCOSC: Изменение среды объясняет геномные вариации африканской лесной лягушки | |
Даже широко распространенные виды могут оказат... | |
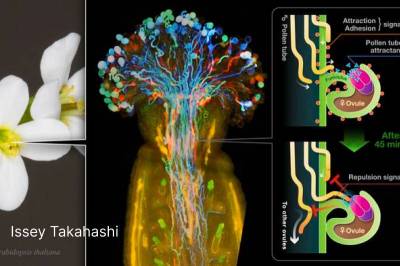 | |
| EMBO Reports: Растения-однолюбы находят одного партнера на всю жизнь | |
Группа ученых из Университета Нагоя, Япон... | |
 | |
| PNAS: Огненные муравьи вдохновили на создание идеального адаптивного материала | |
Огненные муравьи создают плоты, чтобы пережить... | |
 | |
| Nature: Орангутан первым среди животных лечился припаркой из целебных трав | |
Орангутан с острова Суматра удивил ученых... | |
 | |
| Frontiers in Bee Science: Жара мешает шмелям полноценно размножаться | |
В результате климатического кризиса глобальное... | |
 | |
| Низкоинтенсивный выпас лучше для биоразнообразия, но не для землепользователей | |
Выпас как домашних, так и диких... | |
 | |
| Journal of the AChemSociety: Синтетика вызывает хаос в первичном бульоне | |
Наше тело состоит из триллионов различных... | |
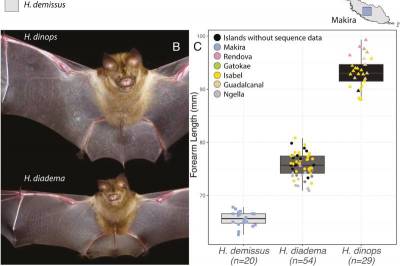 | |
| Evolution: Островные летучие мыши одного вида эволюционируют по-разному | |
Исследователь из Мельбурнского университе... | |
 | |
| ACS Nano: Зубы нутрий и бобров помогут ученым вывести формулу совершенной эмали | |
Болтливые белки, очаровательные нутрии и ... | |
 | |
| New Phytologist: Сети прожилок на листьях появились 201 млн лет назад | |
По мнению исследовательской группы под ру... | |
 | |
| GBE: ДНК древних пингвинов Адели выявило повторы возрастом сотни миллионов лет | |
Микросателлиты — ценный инструмент ... | |